معرفی بیوفیلم
تعریف کلاسیک بیوفیلم آن را به عنوان مجموعه متراکم از باکتریهایی که در سطحوح رشد میکنند نامیده میشود. بیوفیلمها، جوامع پویایی هستند که در ماتریسی محافظتی و خود ساخته از قند و پروتیئن ها زندگی میکنند.
ماهیت سطحی بیوفیلم ها باعث تغییراتی در بیان ژن باکتریها شده که بیوفیلم را از زخم عفونی استاندارد متمایز میکند.
بیوفیلمها بواسطه مقاومت خاص شان در برابر آنتی بیوتیک و بیو اسیدها مشخص میشوند و در عین حال در مقابل سیستم ایمنی میزبان نیز مقاومت میکنند (IWII, 2016). تشکیل بیوفیلم میتواند تحت تاثیر عوامل زیست محیطی نیز قرار گیرد مانند در دسترس بودن اکسیژن و مواد مغذی (ماریس و ورانش، ۲۰۰۷).
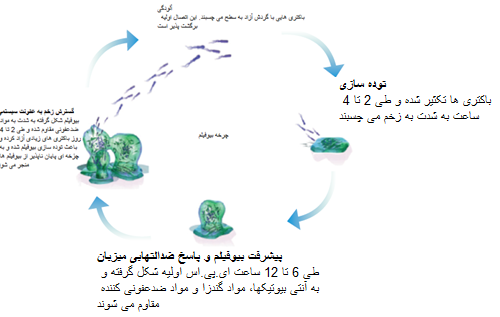
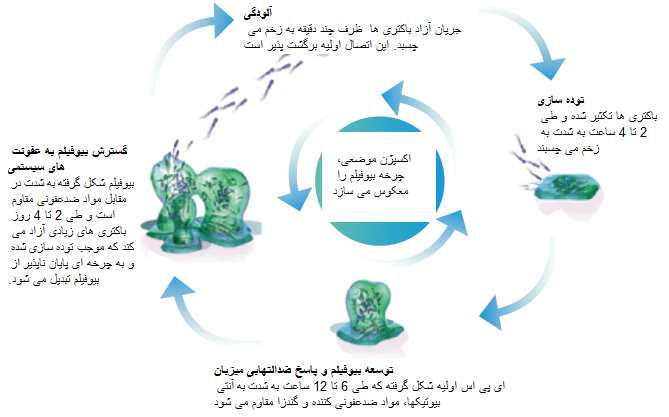
بیوفیلمها در عرض چند ساعت تشکیل شده و پس از ۲ تا ۴ ساعت توده سازی اولیه، به شدت به مولفههای ماتریس خارج سلولی یا بستر زخم میچسبد و برداشتن آنها با شستشوی زخم و حذف بافت مرده (دبریدمان) به سختی انجام میشود (سوانسون و همکاران، ۲۰۱۴).
با پیشروی تشکیل بیوفیلمها، باکتریها نسبت به آنتی بیوتیکها، مواد ضدعفونی کننده و گندزدا مقاومت بیشتری پیدا کرده و از بین بردن آنها با مشکل مواجه میشود. اما همه بیوفیلمها بد نیستند، بیوفیلمهای بیماریزا، مضر بوده و بهبود زخم را به تاخیر میاندازند.
بیوفیلم و مزمن شدن زخمها
بیوفیلمهای بیماریزا، مانع مهمی در بهبود زخم هستند. به این ترتیب، بیوفیلم به مزمن شدن زخمها مرتبط است و علت اصلی عدم بهبود زخمهای مزمن و درمان نشده تلقی میشود. برآورد وجود بیوفیلم، متنوع است ارقام موجود، وجود بیوفیلم در ۶۰ تا ۱۰۰% زخمهای درمان نشده را نشان میدهد. به نظر میرسد شیوع حقیقی آن نزدیک به ۱۰۰% است (WUWHS, 2016).
روشهای سنتی از بین بردن بیوفیلمها عبارتند از:
- برداشت بافت مرده (دبریدمان)
- مواد ضدعفونی کننده یا مواد ضدمیکروبی مرسوم
- آنتی بیوتیکهای سیستماتیک
با این حال، حذف بیوفیلم (و جلوگیری از تشکیل بیوفیلم) کار دشواری است. توده باکتریایی که در بیوفیلم زندگی میکند میتواند مقاومت شدیدی نسبت به مواد ضدمیکروبی پیدا کرده و حتی پانسمان نقرهای نیز برای بیوفیلمها چندان تاثیری ندارد (جمال و همکاران، ۲۰۱۵). این بدان معنا است که به راهکارهای جدیدی نیاز داریم به ویژه در مورد افزایش مقاومت بافت نسبت به آنتی بیوتیکها.
چگونگی شناسایی بیوفیلم
بیوفیلم با چشم غیرمسلح قابل مشاهده نیست و هیچ وسیله خاص و معتبری نیز برای تشخیص آن وجود ندارد. در عمل، این بدان معنا است که شناسایی بیوفیلم اغلب به تجربه بالینی و عینی بستگی دارد.
پژوهش در مورد نمونههای زخم، نشان میدهد هیچ شاخص بصری قطعی برای شناسایی بیوفیلم وجود ندارد، اما برخی زخمهای دارای بیوفیلم نیز ویژگیهای مشترکی از خود نشان میدهند (مانند سطح براق و لزج زخم) (IWII, 2016).
عفونتهای مبتنی بر بیوفیلم از عفونتهای حاد متمایز هستند زیرا بیوفیلمها، علامتهای مشخص عفونت را ندارند (تب، قرمزی، تورم و غیره). بسیاری از زخمهایی که با چشم غیرمسلح، سالم و غیرعفونی به نظر میرسند از طریق بررسیهای آزمایشگاهی وجود بیوفیلم در آنها مشخص شده و درمان زخم متوقف میشود؛ بیوفیلم در بافت عمیق زخم شکل میگیرد و به همین دلیل قابل مشاهده نیست (IWII, 2016). درحالیکه بیوفیلمها ظاهر بالینی متفاوتی دارند اما همچنان عفونتهای مبتنی بر بیوفیلمها، بیماری زا هستند.
بنابراین بهتر است فرض کنیم در کلیه زخمهای مزمن، بیوفیلم وجود دارد:
- درمانهای ضد میکروبی مناسب با شکست مواجه میشوند
- درمان با وجود مدیریت مطلوب زخم و حمایتهای سلامتی، به تعویق میافتد
- تشکیل نسج گرانوله به ندرت رخ میدهد یا گرانوله شکننده ایجاد میشود
- التهاب مزمن در سطح اندکی رخ میدهد ولی رطوبت و ماده اگزودا زیادی وجود دارد.
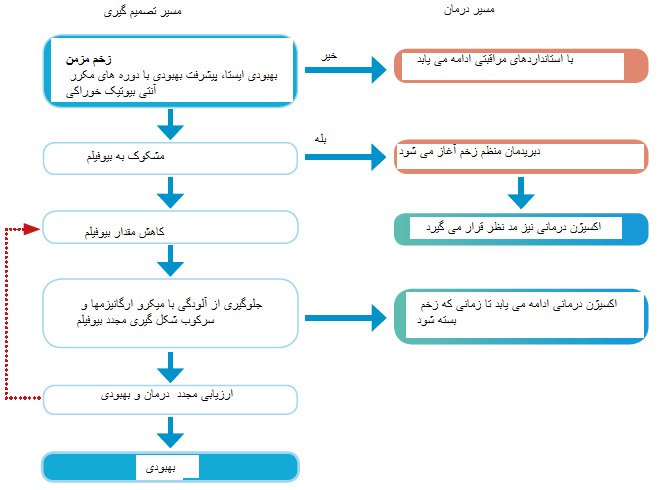
نقش اکسیژن برای درمان زخم
اکسیژن برای درمان زخم در کلیه مراحل بهبودی، حیاتی است و هیپوکسی (فقدان اکسیژن) تاثیر خاصی بر مزمن شدن زخم دارد. در میان تاثیرات هیپوکسی میتوان به فعالیت کاهش یافته ضدمیکروبی فاگوسیتها (بیگانه خوار) اشاره کرد که به دلیل کاهش محافظت ROS رخ میدهد (زخمها، بریتانیا ۲۰۱۷). میزان پایین اکسیژن، توانایی سلولهای ایمنی برای تولید گونههای واکنش دهنده اکسیژن را با مشکل مواجه میکند که برای کشتن باکتریهای که در زخم تجمع کردهاند استفاده میشود، و این خطر تشکیل بیوفیلم را افزایش میدهد. با رشد باکتریها، آنها هنوز هم از اکسیژن و هیپوکسی وخیم استفاده میکنند تا چرخهای بدخیم که بهبود نمییابد ایجاد کنند.
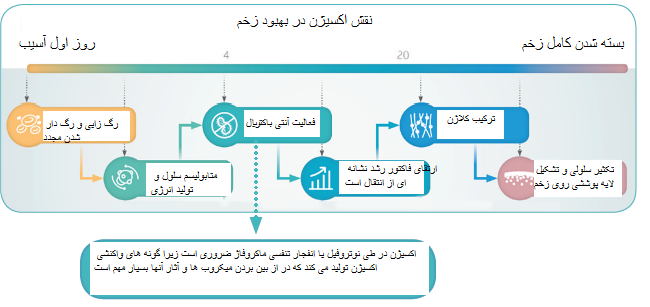
زخمهای مزمن با بیوفیلمهای کامل، نیازمند اقدامات بیشتری هستند تا توازن اکسیژن محلی حفظ شود.
نقش بالقوه اکیسژن موضعی در مدیریت بیوفیلمها
نقش ناتروکس
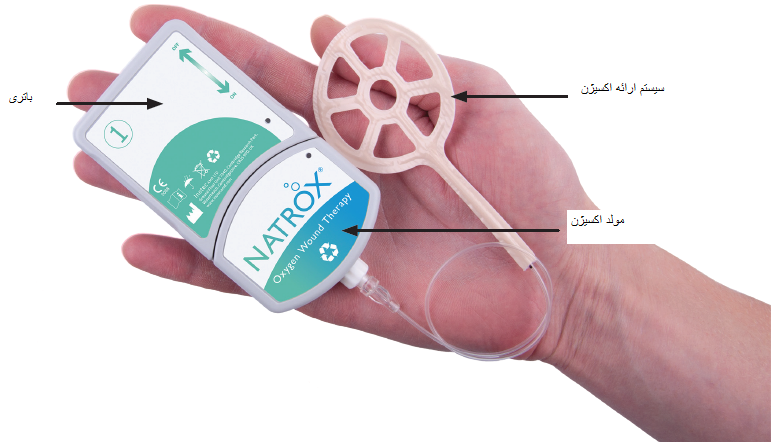
اکسیژن درمانی زخم با ناتروکس (شرکت اینوتک AMD با مسئولیت محدود) یک دستگاه ابتکاری، ساده و سبک وزن است که به لحاظ بالینی تا ۹۸% توانسته اکسیژن مرطوب و خالص را مستقیماً به بستر زخم وارد کند. ثابت شده که این دستگاه، تاثیر مثبتی بر بهبود انواع متنوع زخمهای مزمن و مقاوم به درمان داشته است. این دستگاه نوظهور نشان داده که میتواند ابزاری مفید در مسیر مدیریت بیوفیلمها باشد.
این دستگاه، با ارائه درمانی فعال در طی ۲۴ ساعت شبانه روز و ۷ روز هفته به درمان زخمها کمک میکند. این دستگاه قابل حمل، بی صدا و دارای باتری به بیمار کمک میکند تا فعالیتهای روزمره زندگی خود را با حداقل تداخل انجام دهد.
بررسی یافتهها
Natrox RCT بهترین شیوه استاندارد مراقبتی
یک آزمایش تصادفی جدید و کنترل شده (RCT)، تاثیر اکسیژن درمانی با ناتروکس را با بهترین شیوه استاندارد مراقبتی در بیمارانی با زخم پای دیابتی درمان نشده (DFUs) مقایسه کرد (یوو و همکاران، ۲۰۱۶). یک گروه از بیماران به مدت ۸ هفته با درمان ناتروکس، با یک گروه از افراد که مراقبتهای استاندارد دریافت میکردند مد نظر قرار گرفتند. هر دو گروه، هر هفته از نظر میزان درمان مورد سنجش قرار میگرفتند.
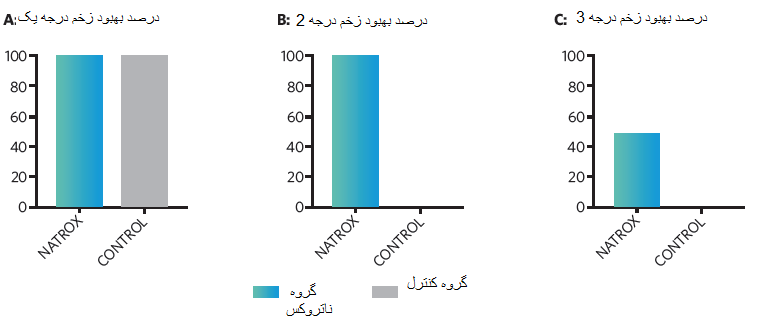
زخمها براساس سیستم دستهبندی زخم دیابتی در دانشگاه تگزاس، درجه بندی شدند و بین درجات ۰ تا ۳ قرار گرفتند. در ابتدا، گروهها به خوبی از نظر اندازه و مشخصههای جمعیتی هماهنگ بودند. ناتروکس در بهبود زخم تاثیر مثبتی داشت حتی برای مقاومترین زخمها. مطالعه ما نشان داد زخم درجه یک با مراقبتهای استاندارد بالینی درمان میشود. افزودن درمان ناتروکس برای بهبود زخمهای درجه ۲ و ۳ تفاوت قابل توجهی ایجاد کرد. بهبودی سریعتر اتفاق افتاد و طی دو هفته پیشرفتهای خاصی در درمان زخم رخ داد.
مطالعه بیوفیلم ناتروکس
با مشاهده تاثیر سریع ناتروکس بر زخمها، تحقیقات پیگیری درمان نیز انجام شد تا تاثیر اکسیژن موضعی بر بیوفیلم برآورد شود. بیمارانی انتخاب شدند که بیش از ۴ هفته و کمتر از ۵۲ هفته دارای DFU بودند. اکسیژن درمانی زخم با ناتروکس به مراقبتهای استاندارد آنها افزوده شد. هر هفته از زخمها عکسبرداری شده و از روی آنها با پنبه نمونه برداری می شد تا از طریق توالی ۱۶S rDNA بیوفیلم آن تحلیل شود. فراوانی باکتریایی مرتبط برای بیشترین فراوانی گونه ۱% تعیین شد و براساس عادت تنفسی دستهبندی شد.
در افرادی که به درمان پاسخ ندادند، میکروبیوم زخم، غیرهوازی و بدون تغییر بود. با این حال، در بیمارانی که زخمشان بهبود یافت، میکروبیوم زخم در دوره درمان ناتروکس تغییر کرد و به یک فلور منتقل شد که تحت سلطه گونههای هوازی قرار داشت.
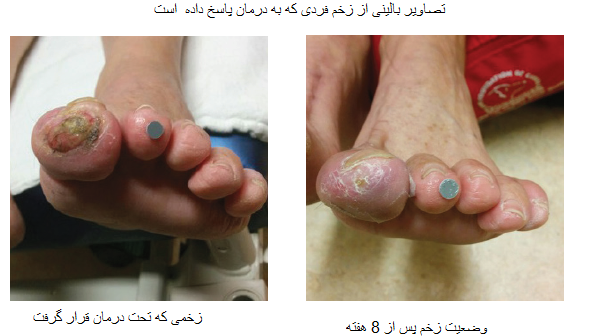
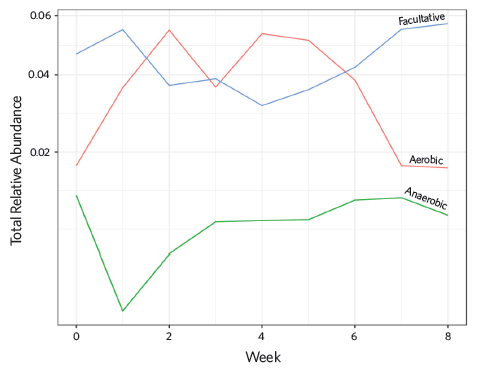
تحلیل توالی گونه بیوفیلم زخم در گذر زمان، براساس عادت تنفسی دسته بندی میشود. تقریباً یک نمود برابر از گونههای هوازی و غیرهوازی در زمان صفر وجود دارد (پیش از اعمال ناتروکس) اما اکسیژن موضعی باعث افزایش سریع در تعداد گونههای هوازی میشود که در هفته دوم در زخمها دیده شدند. غیرهوازیهای دو گونه زیست، مانند استافیلوکوک ها، با اعمال اکسیژن موضعی از تنفس غیرهوازی به تنفس هوازی تبدیل میشوند به طوری که فراوانی کلی آنها در زخم ها با گذشت زمان، تغییر خاصی نداشت.
نکات عملی و مهم
- اگر زخم مشکوک به بیوفیلم باشد به مراقبتهای استاندارد از زخم جواب نمیدهد (کاهش ۴۰ تا ۵۰ درصدی در وسعت زخم پس از ۴ هفته) پس درمان با ناتروکس را مد نظر قرار دهید.
- در اولین دو هفته پس از درمان با ناتروکس، اگزودا یا ترشح زخم افزایش مییابد. با توجه به این تغییرات، انتخاب پانسمان و تغییر پانسمان به منظور تطبیق با افزایش ترشح باید مد نظر باشد. پس از هفته دوم، میزان اگزودا باید کاهش پیدا کند.
- همچنین ممکن است در ابتدای درمان و در دو هفته ابتدایی، وسعت زخم افزایش پیدا کند، پیش از اینکه کوچک شدن و روند بسته شدن زخم آغاز شود.
- مهم است که زخم پیش از درمان، از طریق رژیم آمادهسازی ساختاریافته بستر زخم، به اندازه کافی آماده شود (مانند تایم، داوست و نیوتن، ۲۰۰۵) تا مطمئن شویم زخم کاملاً تمیز شده و تماس کامل میان دستگاه و بستر زخم ایجاد میشود.
- مهم است که از پوست محافظت شود (مانند محافظت از آسیب ناشی از فشار). لوله گذاری باید با دقت انجام شود و ممکن است به بالشتکی نیز نیاز داشته باشد که بهتر جایگذاری شود، به ویژه در مراحل اولیه درمان و زمانی که همراه با تخلیه زخم صورت میگیرد (در زخم پای دیابتی) یا درمان کمپرس انجام میشود (در زخم های وریدی پا).
- ناتروکس نباید همراه با پماد یا سایر درمانهای موضعی مشابه انجام شود زیرا مانعی برای جذب اکسیژن توسط زخم محسوب میشوند.
- پس از بسته شدن زخم، بهتر است درمان تا مدت کوتاهی ادامه یابد تا مطمئن شویم پوست بطور کامل درمان شده و خطر عود مجدد کاهش یافته است؛ بهتر است از مدل Leg Club استفاده کنیم که زخم را بطور رسمی تا ۲ هفته پس از بسته شدن آن، درمان شده تلقی نمیکند که دلیل آن شکنندگی بافت بهبود یافته است (لیندسی، ۲۰۰۴). مدل Leg Club به زخمهای وریدی پا مربوط است اما مفهوم آن در سایر انواع زخمهای مزمن نیز مفید است.
خلاصه مطالب زیست لایه (بیوفیلم)
بیوفیلمها در اکثر زخمهای مزمن مشاهده میشوند و باعث تعویق درمان یا عدم درمان زخم میشوند (WUWHS, 2016). اکسیژن درمانی موضعی، به ویژه به شکل دستگاههای قابل حمل باعث میشود بطور مداوم، اکسیژن، به شیوهای که به بیمار آسیب نرساند به زخم وارد شود و این روش برای بهبود زخمهای مقاوم به درمان و زخمهای درمان نشده بسیار مفید است (هاردینگ، ۲۰۱۶).
شواهد نشان میدهد استفاده از روش اکسیژن درمانی زخم با ناتروکس، تاثیر مثبتی داشته، هم برای زخمهای مقاوم به درمان و هم در تغییر محیط زخمهایی که دارای بیوفیلم هستند. بنابراین، ناتروکس در زخمهای مقاوم به درمان به عنوان بخشی از یک رژیم مراقبتی برای زخمهای دارای بیوفیلم، مفید خواهد بود.